血液内科
主な対象疾患
- 悪性リンパ腫
- 急性骨髄性白血病(AML)
- 急性リンパ性白血病(ALL)
- 慢性骨髄性白血病(CML)
- 骨髄異形成症候群
- 多発性骨髄腫
- 再生不良性貧血
- 特発性血小板減少性紫斑病(ITP)
- 自己免疫性溶血性貧血(AIHA)
- 発作性夜間ヘモグロビン尿症(PNH)
- 重症熱性血小板減少症候群(SFTS)
悪性リンパ腫
悪性リンパ腫とは
悪性リンパ腫は、リンパ球(白血球に属する血液細胞)が腫瘍化し、リンパ節を中心に腫れをつくる病気です。リンパ節以外にも、脾臓、肝臓、胃腸、肺などの臓器や、皮膚、脳、造血の場である骨髄などに病変をつくることもあります。リンパ腫はその性質によって約40種類に細かく分類されます。
リンパ腫の病期
治療に先立って、病期(病変の拡がりの程度)を検査することが必要です。CT検査、PET検査、骨髄検査、血液検査などを行います。その後の治療方針にかかわるので、病期決定は大切なことです。
リンパ腫の治療
リンパ腫の治療の中心は、化学療法と放射線療法です。病期に応じて、これらのいずれか、あるいは併用を行います。場合によっては、さらに治療を工夫した方がよい状況もあります。各々の治療には良い点と悪い点があります。
化学療法
- 抗腫瘍薬(抗がん剤)を点滴や内服で用います。
- 薬剤は全身に行き渡るので、拡がりのあるリンパ腫の治療にも適します。
- 抗腫瘍薬の副作用(後述)が起こる可能性もあります。
- B細胞性リンパ腫の場合には、リンパ腫細胞を狙い打ちにできる抗体薬剤(リツキシマブ)を治療に併用します。
- 約3週間毎に、繰り返し6〜8回の治療を行います。
- はじめは入院での治療を要しますが、可能であれば外来通院治療も考慮できます。
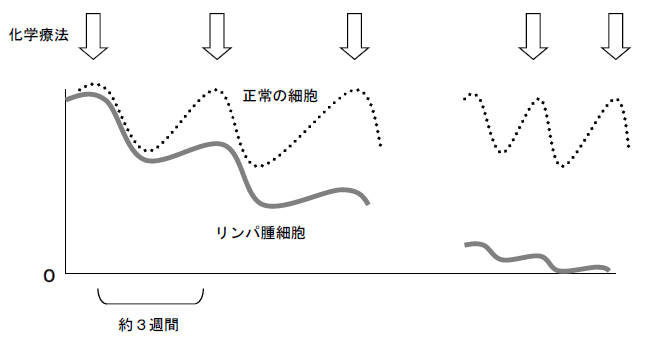
放射線療法
- 一定の範囲をX線照射で狙い打ちする治療です。
- リンパ腫には効果的ですが、照射部位以外の病変には効果はありません。
- 放射線照射の副作用(皮膚炎、血球減少、照射範囲内の近接臓器の障害など)が起こる可能性があります。
リンパ腫の治療成績
- 一般的には、治療により70%程度の方が寛解(検査で病変が消失した状態)に至ります。
- 寛解を得た後に、長期に再発しない方は半数程度の方です。再発した場合には、治療薬や治療方法を変更して再治療が必要になります。
- リンパ腫の種類や性質により治療成績には差があります。
急性骨髄性白血病(AML)
急性骨髄性白血病とは
急性白血病は、白血球(血液細胞のひとつ)が腫瘍化し、異常な白血病細胞として急激に増える病気です。白血病細胞が増えると、正常の造血ができなくなり、貧血や血小板減少をきたします。また、正常の白血球(免疫力を担っている)も減少するため発熱や感染を起こしてしまいます。
急性骨髄性白血病の治療
白血病の治療の中心は、化学療法です。化学療法を繰り返し行なうことで、白血病細胞の根絶を図ります。
化学療法には、抗腫瘍薬(抗がん剤)を点滴や内服で用います。薬剤は白血病細胞だけを狙い撃ちすることはできないので、正常の細胞(正常の血液細胞や臓器)に負担をかけることがあります。そのため、薬剤による副作用が起こる可能性もあります。また、脳や脊髄に白血病細胞が侵入するのを予防するために、抗がん薬の髄腔内投与を行うことがあります。
化学療法の進み方
約4週間毎に繰り返し治療を行い、白血病細胞の根絶を図ります。
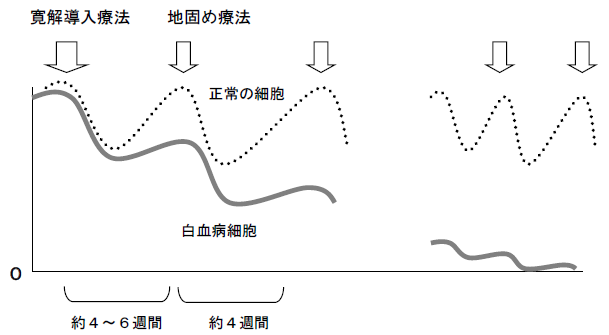
治療成績と治療の工夫
- 化学療法を行なうことで、約70%の方は「見た目に白血病細胞が消失して体調が整う状態(血液学的完全寛解という)」となります。実際には、残存白血病細胞をさらに減らし、より良質の寛解状態を得るために、化学療法を繰返し行ないます。
- その後は、再発しないかどうかを慎重に経過観察します。長期に再発なく経過する方は一般に30〜40%程度です。再発した場合や寛解に至りにくい場合、初診時に難治性の要素をもつ場合には、治療法の工夫が必要となります。
- 根治を得るために、年齢や状況により造血幹細胞移植療法(骨髄移植、末梢血幹細胞移植、臍帯血移植)を考慮することがあります。
急性リンパ性白血病(ALL)
急性リンパ性白血病とは
急性リンパ性白血病は、リンパ球(血液細胞である白血球のひとつ)が腫瘍化し、異常な白血病細胞として急激に増える病気です。白血病細胞が増えると、正常の造血ができなくなり、貧血や血小板減少をきたします。また、正常の白血球(免疫力を担っている)も減少するため発熱や感染を起こしてしまいます。
急性リンパ性白血病の治療
白血病の治療の中心は、化学療法です。化学療法を繰り返し行なうことで、白血病細胞の根絶を図ります。化学療法には、抗腫瘍薬(抗がん剤)やステロイドホルモン剤を点滴や内服で用います。薬剤は白血病細胞だけを狙い撃ちすることはできないので、正常の細胞(正常の血液細胞や臓器)に負担をかけることがあります。そのため、薬剤による副作用が起こる可能性もあります。
化学療法の進み方
約4週間毎に繰り返し治療を行い、白血病細胞の根絶を図ります。
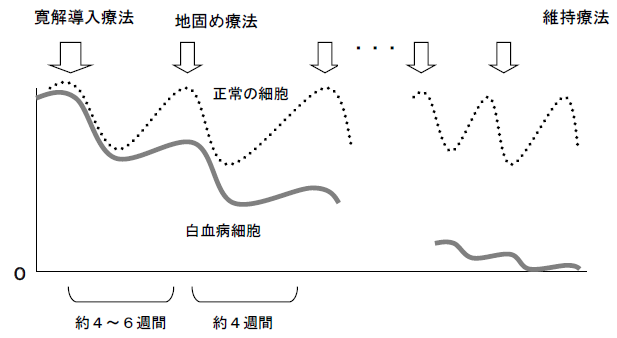
治療の効果と工夫
- 化学療法を行なうことによって、約70%の人は「見た目に白血病細胞が消失して体調が整う状態(血液学的完全寛解という)」となります。実際には、残存白血病細胞をさらに減らし、より深い寛解状態を得るために、化学療法を繰り返し行ないます。
- その後は維持療法を行いながら、再発しないかどうかを慎重に経過観察します。長期に再発なく経過する方は一般に25〜40%程度です。再発した場合や治りにくい場合、また白血病が難治性の要素をもつ場合には、治療法の工夫が必要となります。
- 十分な根治を得るために、年齢や状況により造血幹細胞移植療法(骨髄移植、末梢血幹細胞移植、臍帯血移植)を考慮した方がよい場合があります。造血幹細胞移植はリスクも伴う治療なので、行った方がよいかどうかには十分な検討が必要です。
- フィラデルフィア染色体異常という特有の染色体異常を有する場合には、この染色体異常により生じるBCR/ABL遺伝子異常を狙った分子標的薬であるイマチニブ、ダサチニブ、ポナチニブなどを使用して治療します。
慢性骨髄性白血病(CML)
慢性骨髄性白血病とは
慢性骨髄性白血病は、血液のもとになる細胞(造血幹細胞)にフィラデルフィア染色体異常という特殊な遺伝子異常が生じることによって、異常な血液細胞が腫瘍性に増加する病気です。とくに白血病細胞として白血球が増えることが特徴的です。発症からしばらくの間はあまり症状がなく経過しますが、最後には急性白血病のような病状になります。
慢性骨髄性白血病の自然経過
慢性骨髄性白血病は、慢性期、移行期、急性転化期の3つの時期に分けられます。
慢性期
- 発症から5年ほどの間は、ほとんど症状がなく経過します。
- 血液検査で白血球数が増加したり、脾腫がみられたりします。
- 慢性期は症状がないので、近年は健診で発見されることも多いです。
移行期
- 未熟な白血病細胞(芽球)が増加したり、脾腫が増悪したりします。
急性転化期
- 発症から5〜10年後には、急性白血病のような病状になり、急激に病状が悪化して体調が崩れます。
- 急性転化した場合には、治療が効きにくくなります。
慢性骨髄性白血病のくわしい病態
- フィラデルフィア染色体異常が白血病化に関わっています。この染色体異常は9番染色体と22番染色体の一部が相互に入れ替わって起こります。これにより、BCR/ABL融合遺伝子が生じると、ABLチロシンキナーゼという酵素の働きが亢進して、白血病細胞が増えてしまいます。
- 治療により白血病細胞が徐々に減少します。顕微鏡でも確認できないくらい減少した以降は、血液検査でこのBCR/ABL融合遺伝子の量を測定することで、体内に残っている白血病細胞を微小なレベルで調べることができます。
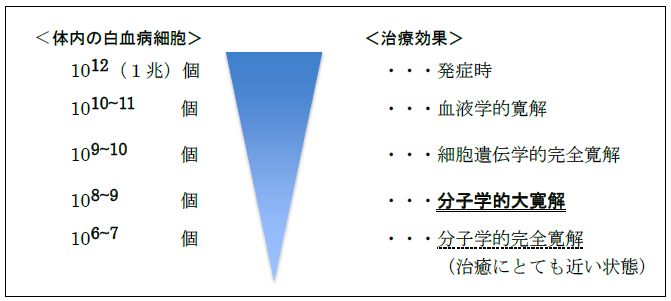
- 分子学的大寛解(MR 3, MMRともいう)とは、発症時を100%とすると白血病細胞が0.1%以下の状態をいいます。分子学的大寛解を達成すると、治療を継続すれば白血病が悪化することはほとんどなくなります。
- MR4, 4.5, 5(それぞれ0.01%, 0.0032%, 0.001%)といった、さらに深い寛解状態を得ることが、近年はより好ましいとされています。
慢性骨髄性白血病の治療
1) 慢性骨髄性白血病に対する特効薬(ABLチロシンキナーゼ阻害薬)が開発され、これまでに比べて治療成績が飛躍的に改善しています。
- ダサチニブ、ニロチニブ、イマチニブのうち、最も適した薬剤を使用します。
- 治療薬は内服薬で、外来治療が可能です。毎日の内服が長期に必要です。
- 治療により、約80~90 %以上の人に細胞遺伝学的寛解をこえる効果が期待されます。
- 治療の目標は、「できるだけ分子学的大寛解以上の効果を得ること」です。効果が不十分な場合は薬剤の変更を行うことがあります。
- 治療薬の副作用や効果不良の場合には、他の薬剤(ボスチニブ、ポナチニブなども含む)に変更します。
2) 病期が移行期や急性転化期である場合、白血病細胞に薬剤耐性が生じてチロシンキナーゼ阻害薬が無効の場合、薬剤が体に合わない(不耐容という)場合には、造血幹細胞移植(いわゆる骨髄移植)を考慮することがあります。
- 造血幹細胞の提供者(ドナー)が必要です。
- 高齢の方(55歳以上)や合併症のある方には一般には勧められません。
3) 極めてよい寛解状態が長く持続した場合には、チロシンキナーゼ阻害薬の内服治療を終了することができるかもしれません。
- まだ研究的な段階の試みであり、原則的には治療の継続が必要です。中止した患者さんの約半数は治療効果が維持されますが、半数は再発して再治療を要することも分かっています。
骨髄異形成症候群
骨髄異形成症候群(MDS)とは
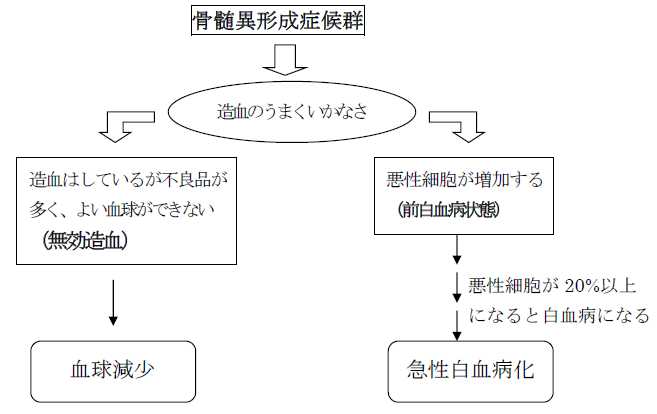
骨髄異形成症候群は、造血の場である骨髄で造血がうまくできなくなる疾患です。造血のうまくいかなさには、①骨髄では血球を造ろうとしているが不良品の血球ができてしまう[無効造血]、②腫瘍性に悪性細胞をつくるようになる[前白血病状態]、という2つの特徴があります。このことから、骨髄異形成症候群は血液悪性疾患のひとつといえます。
骨髄異形成症候群の治療
骨髄異形成症候群の治療は、病状により以下の治療法から最適な方法を選択して行ないます。しかしながら、骨髄異形成症候群は完全には治りにくい疾患でもあり、治療を行ないながら病気と付き合うことも必要となります。
① 輸血療法
- 不足する赤血球と血小板を定期的な輸血で補います。
- 赤血球輸血を繰返すと体内に鉄分が過剰になるため、鉄の排泄促進薬(デフェラシロクス)を併用することがあります。
② 赤血球造血ホルモン療法
- 貧血に対して赤血球造血ホルモン(ダルベポエチン)を注射して、造血の改善を図ります。
③ ビタミン剤や副腎皮質ホルモンの使用
- 治療効果は大ではありませんが、内服薬なので外来治療が可能です。
- ホルモン剤により、男性化・血糖の上昇(糖尿病)などが生じることがあります。
④ アザシチジン療法
- 約4週間ごとに7日間(5日間のこともある)注射を行ないます。
- 血球減少を改善させ輸血頻度を減じたり不要にしたりする効果、および白血病化を遅らせる効果が期待されます。
⑤ 免疫抑制療法
- 血球減少が主な症候であれば、シクロスポリンなどの免疫抑制剤が造血力の改善に効果がある場合があります。
⑥ 化学療法
- 白血病化しつつある場合や、白血病化している場合には、急性白血病に準じた化学療法を行ない、悪性細胞を減少させます。
⑦ 造血幹細胞移植療法(骨髄移植、臍帯血移植など)
- 骨髄異形成症候群を根治する可能性のある唯一の方法です。
- 血液のもとになる造血幹細胞を提供してくれるドナーが必要です。
- 移植療法は治療に関連する副作用も大きいことから、65歳以上の方や臓器障害がある方には推奨されません。
多発性骨髄腫
多発性骨髄腫とは
多発性骨髄腫は、形質細胞(免疫抗体を産生し免疫機能を担う血液細胞)が腫瘍化し、骨髄を中心に増殖する病気です。血液悪性腫瘍、いわゆる血液がんのひとつです。一般的に骨髄腫は病気の進行が比較的緩やかな疾患ですが、現在の治療法では根治させることがまだ困難な疾患でもあります。
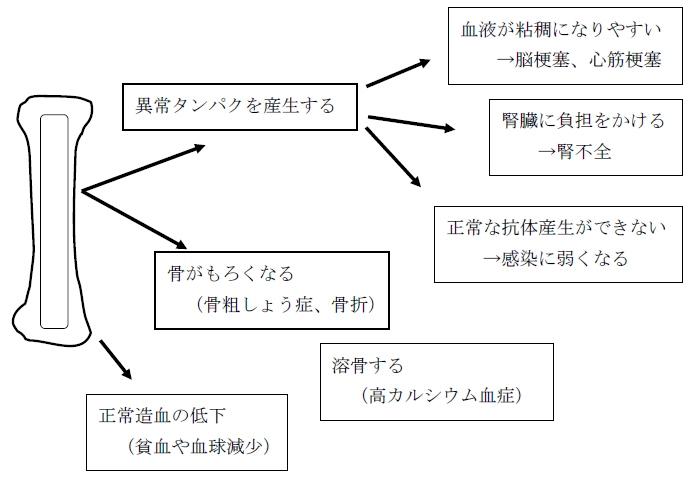
多発性骨髄腫の病状
多発性骨髄腫の病期
治療に先立って、病期(病変の拡がりの程度)を検査することが必要です。
骨髄検査、血液検査、骨シンチグラフィ検査、PET検査、全身レントゲン検査などを行います。その後の治療方針にかかわるので、病期決定は大切なことです。
骨髄腫の治療
骨髄腫の治療の中心は、化学療法です。近年、骨髄腫に対して効果の高い薬剤が使用できるようになってきました。年齢や病状に応じて、また各々の治療の良い点と悪い点を考慮して、最適な治療を選択します。深い寛解を得ることとその寛解期間をより長く維持することが治療の目標です。
化学療法
古くからの治療:現在は第1には行わないことが多い
i) 経口化学療法(MP療法)
- 4〜6週間ごとにメルファランとプレドニゾロンの内服治療を行なう
- 効果発現は緩やかだが、外来治療ができる
ii) 大量ステロイド療法(デキサメタゾン療法)
- 大量のステロイドホルモンを継続的に投与する
iii) 多剤併用化学療法(VAD療法など)
- 数種類の抗腫瘍薬とステロイドホルモン剤を併用した点滴療法
- 効果発現は速やかだが、治療には入院を要する
条件が許せば考慮するべき治療
iv) 自家末梢血幹細胞移植を併用した大量化学療法
- 大量の抗腫瘍薬(メルファラン)を用いて治療を行なう
- 化学療法後の造血機能の救援のため、自家末梢血幹細胞移植の併用が必須
- 65才までが一般的だが、70歳くらいまでの方には施行可能な治療法
現在の標準的治療(下線が第1選択)
v) ボルテゾミブ療法
- プロテアソーム阻害薬という新しい効果を持つ抗腫瘍薬
- デキサメタゾンやシクロフォスファミドなどと併用する注射薬です
- 副作用に、神経障害、血球減少、重篤な間質性肺炎などがある
vi) サリドマイド療法
- 内服治療(1-2錠/日)で、難治性骨髄腫に30%程度の奏効率がある
- 管理手順を守り十分な留意が必要で、治療中は避妊が必須です
- 副作用は比較的少ないが、便秘、静脈血栓症、神経障害などがある
- MP療法やボルテゾミブと併用することもある
vii) レナリドミド療法
- デキサメタゾンや他の薬剤と併用して用いる経口薬です
- 1サイクル(28日間)のうち21日間の内服を行う
- サリドマイド誘導体であり、サリドマイド同様の管理手順の遵守が必要
- 神経障害は少ないが、血球減少、静脈血栓症、腎障害、皮疹などの懸念はある
効果が不十分な場合の治療
viii) カーフィルゾミブ療法
- 新しいプロテアソーム阻害薬のひとつ
- レナリドミド、デキサメタゾンと併用する注射薬です(レナリドミドは用いないこともある)
- 副作用に心障害、間質性肺炎、血球減少、末梢神経障害などがある
ix) イキサゾミブ療法
- 新しいプロテアソーム阻害薬のひとつ
- レナリドミド、デキサメタゾンと併用する週1回の内服薬です
- 副作用に下痢、血球減少、末梢神経障害などがある
x) エロツズマブ療法
- 骨髄腫細胞とNKリンパ球(免疫作用にかかわるリンパ球)に発現しているSLAMF7という物質に結合する抗体医薬で、免疫作用を高めて骨髄腫細胞を減らす効果があります
- レナリドミド、デキサメタゾンと併用する注射薬です
- 副作用にインフュージョン・リアクション(注射時反応)があり、予防薬が必要です
xi) ポマリドミド療法
- レナリドミド誘導体で、内服方法も管理手順もほぼ同様の内服薬です
- デキサメタゾンと併用して用います
- レナリドミドと同様に血球減少、静脈血栓症、皮疹などの懸念はある
xii) パノビノスタット療法
- ボルテゾミブ、デキサメタゾンと併用する内服薬です
- 副作用で、多くの場合に下痢がみられます。場合によっては止痢剤を併用する
放射線療法
- 一定の範囲をX線で狙い打ちする治療です
- 骨髄外腫瘤、骨痛に対して有効なことが多いです
骨病変に対する支持療法
- 新しい骨折を予防するために、ビスホスホネート製剤あるいはデノスマブを定期的に使用します
- 骨痛に対しては、鎮痛薬(モルヒネ製剤が主体)を使用することがあります
再生不良性貧血
再生不良性貧血とは
再生不良性貧血は、血液細胞(赤血球、白血球、血小板)の産生が全般にできなくなってしまう病気です。造血力が低下する原因のひとつに、造血のもとになる造血幹細胞に対して、自分自身の免疫力が間違えて攻撃をしてしまうことがあります。この自分自身を攻撃してしまう病態を「自己免疫」といいます。この自己免疫機序には、免疫機能を担っているTリンパ球がおもに関わっていると考えられています。
再生不良性貧血の症状
血液細胞の減少により、下記のような症状が出現します。

* 好中球が 500/ μlを下回ると重症感染の危険が高まりす。 を下回ると重症感染の危険が高まりす。
* 血色素量( Hb )が 7〜8 g/dlg/dl を下回ると輸血が必要になってきます。 を下回ると輸血が必要になってきます。
* 血小板減少が進行すると 出血症状が現します。
診断と検査
血液検査のほかに、造血の場である骨髄の状態を調べるための骨髄検査や骨髄MRI検査を行い診断します。また、血球減少をきたす他の病気が隠れていないかを調べるための検査も必要に応じて行います。再生不良性貧血は、厚生労働省の特定疾患に該当しますから、診断後には届出を行います。
再生不良性貧血の原因と重症度
この病気を発症する主な原因は分かっていませんが、その一部に、肝炎に合併して発症するもの、薬剤により発症するもの、発作性夜間ヘモグロビン尿症(PNH)に合併するものなどがあることが知られています。
再生不良性貧血は、血球減少の程度により軽症から最重症まで分類されます。重症度により、適した治療法が選択されます。
再生不良性貧血の治療
再生不良性貧血の治療の中心は、自分自身の造血を妨げている間違えた免疫力(自己免疫)を抑えることにあり、こういった治療を免疫抑制療法といいます。軽症例には造血を促すホルモン剤治療、重症例の若年者には造血幹細胞移植(骨髄移植など)が行なわれることもあります。
主に軽症〜中等症に行なわれる治療法
① 蛋白同化ホルモン(ステロイド)療法
- 造血力を賦活する治療です
- ホルモン剤により、男性化・血糖の上昇(糖尿病)などが生じることがあります
- 治療効果は大ではありませんが、内服薬なので外来治療が可能です
主に中等症〜重症に対して行なわれる治療法
② シクロスポリン療法
- 免疫抑制療法のひとつです
- 1日2回、12時間ごとに内服します
- 単独で用いた場合の奏効率は30〜40%程度です
- 薬剤の副作用に、腎障害、肝障害、感染症などがあります
③ 抗胸腺細胞グロブリン(ATG)療法
- 免疫抑制療法のひとつです
- 5日間の点滴治療で、多くはシクロスポリンやステロイドホルモンと併用します
- ウサギを免疫して作製される抗血清製剤です
- 副作用として、皮疹、発熱、血小板減少が多くの方に出現します
- ときに、重篤なアレルギー反応(アナフィラキシーという)、全身性紅斑、むくみ、腎障害などの副作用があります
- 奏効率は単独で30〜40%で、通常は1、2ヶ月で効果が出ますが、効果発現までに3〜6ヶ月を要することもあります
- シクロスポリンとの併用で奏効率が60~70%に高まります
④ 顆粒球コロニー刺激因子(G-CSF)療法
- 白血球減少に対して使用する造血ホルモンです
- 抗胸腺細胞グロブリンやシクロスポリンと併用することもあります。
⑤ 造血幹細胞移植療法
- 造血力を根本的に改善するために、HLAが一致する提供者(ドナー)から造血幹細胞の移植を受ける治療です
- 治療に伴う合併症があるため、治療を受けられる年齢には制限があります
- 重症/最重症型で若年(40才以下)の方には、免疫抑制療法よりも優先して考慮すべき治療法です
どの病期にも共通する治療法
⑥ 輸血療法
- 不足する赤血球や血小板を輸血で補います。
- 輸血に伴うアレルギーや感染症のリスクはありますが、血球数の増加を図るには大変有効な方法です。
- 頻回に赤血球輸血を行なうと鉄過剰症を合併します。治療と予防のために鉄キレート剤(除鉄剤)を内服することがあります。
特発性血小板減少性紫斑病(ITP)
特発性血小板減少性紫斑病(ITP)とは
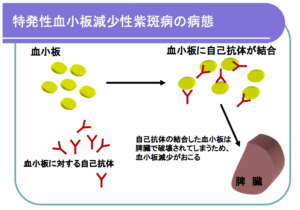
特発性血小板減少性紫斑病は、血小板の産生には大きな異常はありませんが、自分自身の血小板を自分自身が間違えて攻撃してしまうことにより、血小板が減少してしまう病気です。
この自分自身を攻撃してしまう病態を自己免疫といい、ITPでは血小板に対して自己抗体をつくってしまいます。自己抗体が結合した血小板は、脾臓などで破壊・処理されてしまいます。
ITPは、厚生労働省の特定疾患(いわゆる難病指定)に該当しますから、診断後には届出を行います。
血小板減少による症状
血小板は止血の役目を担っています。血小板減少が進行すると、皮下出血、鼻出血、口内出血など、種々の出血症状が出現します。脳出血、肺出血、腹腔内出血などは生命に関わる重篤な出血です。
ITPの病型分類
ITPは発症から6ヶ月以内を急性型、6ヶ月以上経過したものを慢性型といいます。
急性型はウイルス感染を契機に発症することがあります。急性型の多くは、6ヶ月以内に血小板数が改善しますが、一部は慢性型に移行してしまいます。慢性化するかしないかは、初期には見分けられません。
慢性型の多くの原因は分かっていませんが、その一部にヘリコバクター・ピロリ感染があることが最近明らかになりました。
ITPの治療
標準的に行なわれる治療法
① 副腎皮質ホルモン(ステロイド)療法
- 自己抗体の産生を抑制する標準的な治療
- 治療効果は70%くらいありますが、ステロイド剤の減量に際して血小板減少が再燃することもあります
- 治療期間は数ヶ月〜数年以上に及びます
- 副腎皮質ホルモン剤により、肥満・骨粗しょう症・血糖の上昇(糖尿病)・胃潰瘍などが生じることがあります。
② 脾臓摘出療法
- 血小板が壊される主な場所である脾臓を外科的に摘除(開腹手術あるいは腹腔鏡手術)します
- 長期寛解率は60%程度です
- 脾臓摘出により免疫力低下をきたすので、予防的に肺炎球菌ワクチンを接種しておきます
- 術後には薬剤の投与は不要なので、将来妊娠を考える場合などにも適した治療法です。
③ ヘリコバクター・ピロリ除菌療法
- 慢性型ITPの方で、ヘリコバクター・ピロリ菌に感染している場合には、可能であれば第1に除菌療法を行ないます
- 除菌が成功した場合の奏効率は50〜60%です
- 除菌に失敗した場合には、再除菌療法を試みます
大きな出血がある、あるいは出血が予想される場合の治療法
④ 大量免疫グロブリン療法(一時的な治療法)
- 免疫グロブリン製剤を大量に投与すると血小板が破壊されにくくなり、およそ7日目から10日目頃に最も血小板数が増加します
- 効果は速やかですが一時的で、根治治療にはなりません
- 重篤な出血症状がある場合や、手術や出産が予定される場合に行います
治りにくい場合の新しい治療薬剤
⑤ エルトロンボパグ療法
- 血小板産生を強力に促すトロンボポエチン受容体作動薬です
- 1日1回、決められた時間(空腹時)に内服します
- 少量から少しずつ増量していき、必要量を決定します
- 肝障害などを起こす可能性があり、注意が必要です
⑥ ロミプロスチム療法
- 血小板産生を強力に促すトロンボポエチン受容体作動薬です
- 1週間に1回、皮下注射を行ないます
⑦ リツキシマブ療法
- 抗血小板抗体の産生にかかわるBリンパ球に対する抗体医薬です
- 1週間毎に4回投与しますが、初回投与は入院が必要です
- 特に初回投与において、薬剤注入時反応(薬剤に対するアレルギー反応で、発熱や発疹、呼吸困難などがおこる)がみられることがあります。
その他の治療法
標準的治療の効果が不十分な場合は、以下の治療を試みます。各々の奏効率 はそれほど高くはありませんが、試みる価値はあります。
⑧ 免疫抑制療法
- 免疫抑制剤を用いて、自己免疫機序の改善を目指します
⑨ セファランチン療法(自費診療)
- セファランチン内服で血小板が増えることがあります
⑩ 加味帰脾湯(カミキヒトウ)療法
- 漢方薬の内服で時に血小板数が改善した報告があります。
自己免疫性溶血性貧血(AIHA)
後天性自己免疫性溶血性貧血(AIHA)とは
後天性自己免疫性溶血性貧血は、赤血球が破壊(溶血という)される病気のひとつです。この病気では、自分の赤血球に対して自己抗体をつくってしまい、自分自身の赤血球を自分自身の免疫力が間違えて攻撃してしまいます(自己免疫)。自己抗体が結合した赤血球は主に脾臓で破壊され、溶血が生じます。
後天性自己免疫性溶血性貧血の症状
赤血球の破壊による症状

貧血の進行が急で重篤な場合には、心不全、呼吸困難、意識障害などを伴うことがあります。
分類について
この病気には、①基礎疾患があり発症するもの(続発性)、②基礎疾患がなく発症するもの(特発性)があります。基礎疾患として、感染症(細菌やウイルス)、リウマチ性疾患、自己免疫性疾患、悪性腫瘍、悪性リンパ腫などがありますから、これらの合併がないか調べます。なんらかの病気の併存が明らかになればそれに対しての治療が必要になります。
治療について
① 副腎皮質ホルモン(ステロイド)療法
- 自己抗体の産生をおさえるための治療です。
- 治療効果は一般に良好で、約70〜80%は貧血の改善が得られます。
- 徐々に減量しますが、再発を防ぐには少量の維持療法を長期に要します。
- 副腎皮質ホルモン剤により、肥満・骨粗しょう症・血糖の上昇(糖尿病)・胃潰瘍などが生じることがあります。
② 免疫抑制剤
- 副腎皮質ホルモン剤の効果が不十分の場合に、変更したり追加したりすることがあります。
③ 輸血療法
- 貧血が高度の場合(血色素量 5〜6 g/dl以下)には、輸血による赤血球の補充が必要です。
④ 脾臓摘出術
- 副腎皮質ホルモン剤の治療が無効の場合に、最終的な溶血の場である脾臓を外科的に摘出して、溶血を和らげる方法もあります。
発作性夜間ヘモグロビン尿症(PNH)
発作性夜間血色素尿症とは
発作性夜間血色素尿症(PNH)は、慢性的に赤血球が破壊される(溶血という)病気です。血液細胞のもとになる造血幹細胞に突然変異が起こり、異常な赤血球(PNH型赤血球)がつくられますが、この赤血球には自分自身を守るタンパクが欠けているため、健常の「補体による免疫システム」によって容易に攻撃を受けてしまい壊されます。
PNHでは慢性的に溶血が起こり、貧血が進行します。また、血栓症やさまざまな臓器障害を合併することがあります。また、溶血は感染症を合併したときや手術のときに急性増悪することがあります(溶血発作という)。PNHの遺伝子異常は、造血幹細胞に起こるので、赤血球だけでなく白血球や血小板の数が減少すること(造血不全)もあります。
PNHは、厚生労働省の特定疾患(いわゆる難病指定)に該当しますから、診断後には届出を行います。
発作性夜間血色素尿症の症状
① 赤血球の破壊による症状
貧血・・・息切れ、倦怠感、めまい、立ちくらみ など
黄疸・・・皮膚や目が黄色くなる
血尿・・・茶褐色(コーラ色)の尿がでる
② 白血球減少、血小板減少
白血球減少・・・感染を起こしやすくなる
血小板減少・・・出血しやすい、止血しにくい
③ 血栓症による症状
血管内に血栓ができて閉塞をきたします。心筋梗塞や脳梗塞、腹痛(腸を養う血管が詰まる)などを突然きたすことがあります。
④ 腎臓障害
⑤ 肺障害・・・肺高血圧症などで息切れや呼吸苦がおこることがあります
⑥ 勃起不全(ED)
⑦ 嚥下障害
などの多彩な症状がみられます。
発作性夜間血色素尿症の治療
① 副腎皮質ホルモン(ステロイド)療法
- 溶血を抑制する治療
- 効果は軽度〜中等度である。急性増悪時にも有用なことが多い。
- 副腎皮質ホルモン剤により、肥満・骨粗しょう症・血糖の上昇(糖尿病)・胃潰瘍などが生じることがあります。
② タンパク同化ホルモン療法
- 血球産生を促進する治療
- 造血不全があり血球が少ない場合に用いることがある
③ 免疫抑制療法
- 血球産生が低下している場合にシクロスポリンなどの投与を試みることがあります
④ 輸血療法
- 貧血が高度の場合(血色素量 7~8 g/dl以下)には、輸血による赤血球の補充が必要です。
⑤ 補液治療
- 溶血発作が生じた場合には、腎臓を保護するために大量点滴やハプトグロビン(壊れたヘモグロビンの処理を促進する薬剤)の投与を行います。入院が必要です。
⑥ 造血幹細胞移植(骨髄移植)
- 根治する可能性のある唯一の方法です。
- 血液のもとになる造血幹細胞を提供するドナーが必要です。
- 移植療法は治療関連の特殊な副作用も大きいことから、年齢や病状により行わない方がよいことがあります。
⑦ エクリズマブ療法
- 補体システムの一部であるC5という物質を阻害することで赤血球の溶血を強力に抑制する新しい抗体医薬(抗C5抗体)です。
- 高い確率で溶血を抑える効果があります。また、血栓症の発症リスクも低下させたり、倦怠感を改善したりもします。
- 中等度〜重度の溶血がある場合に使用が考慮されます。
- はじめの1か月は毎週、その後は2週ごとの点滴注射薬です。
- 一度投与を始めると、原則的には、ずっとこの注射を継続しなければなりません。
- 免疫機能が抑制されて髄膜炎菌感染に弱くなるため、使用に先立って髄膜炎菌ワクチンを接種して発症を予防します。
重症熱性血小板減少症候群(SFTS)
重症熱性血小板減少症候群(SFTS)とは
SFTSは、中国で見つかったSFTSウイルスによる新興ウイルス感染症です。2006年頃から安徽省、河南省、湖北省の山岳地帯の農夫の間に致死率が12%に及ぶ疾患が流行していることに注目した研究者らが、患者から新種ウイルスを分離しました。流行地域のマダニの約5%がウイルスを保有していたことから、マダニ媒介性感染症と考えられています。当初は中国以外からの報告はありませんでしたが、2013年以降、日本と韓国でも患者が確認されています。
SFTSウイルス(電子顕微鏡写真)

十分に吸血したマダニ
SFTSの症状
発熱、倦怠感、嘔吐や下痢などの消化器症状に血小板減少と白血球減少を伴うことが特徴的です。筋肉痛や脱力、蛋白尿、血尿、下血などもよくみられ、頭痛や意識障害などの神経症状を伴うこともあります。リンパ節腫大もしばしば伴い、特にマダニ刺咬部の所属リンパ節が腫大します。しかし、マダニ刺咬歴がない患者も半数います。最近は、動物からの感染も報告されています。
潜伏期は5~14日間で、発症後1~2週間に血中ウイルス量が極期に達し、上記の症候や検査値異常が進行します。重症例では血球貪食症候群という病態を合併して、多臓器不全に至り死亡します。軽症例では、発症10日目頃から血中ウイルス量が減少に転じて症状が改善していきます。
SFTSの臨床経過
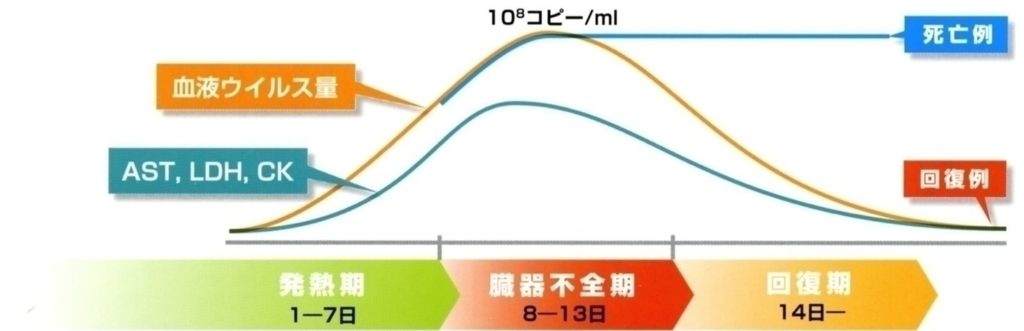
SFTS診療の手引き より
SFTSの治療
現在までのところSFTSに対する特異的治療はないため、重症化に備えて集中治療にも対応できる病院で支持療法を中心に慎重な管理を行います。血球貪食症候群を合併する場合には、ステロイド療法が併用されます。
近年、日本で創薬されたファビピラビルという抗ウイルス薬の有効性が注目されています。当院は、SFTSに対するファビピラビル治療の治験に取り組んでいる、山口県で唯一の医療機関です。
